Луцифераза
Луцифераза е общ термин за клас ензими оксигенази, участващи в биолуминесценцията и различни от фотопротеин. Името произлиза от името на Луцифер, означава „носещ светлина“. Типичен пример е луциферазата (ЕС 1.13.12.7) от светулка Photinus pyralis.[1] „Луцифераза“ като лабораторен реагент често се отнася до Р. pyralis луцифераза, въпреки че рекомбинантни луциферази от няколко други видове светулки са също се ползват в лабораторната практика.

| Обща информация | |
|---|---|
| Символ | Firefly luciferase |
| PDB | , More structures |
| UniProt | |
| Други | |
| Класификация на ензими | |
| Бактериална луцифераза, монооксигеназно семейство | |||||||||||
| Идентификатори | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Символ | Bac_luciferase | ||||||||||
| Pfam | PF00296 | ||||||||||
| InterPro | IPR016048 | ||||||||||
| PROSITE | PDOC00397 | ||||||||||
| SCOP | 1nfp | ||||||||||
| SUPERFAMILY | 1nfp | ||||||||||
| |||||||||||
| Луцифераза в Общомедия | |||||||||||
| Луцифераза от динофлагелати, каталитичен домен | |||||||||||
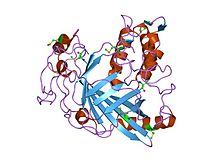 Кристална структура на каталитичен домен на луцифераза от динофлагелата Lingulodinium polyedrum | |||||||||||
| Идентификатори | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Символ | Luciferase_cat | ||||||||||
| Pfam | PF10285 | ||||||||||
| InterPro | IPR018804 | ||||||||||
| |||||||||||
| Луцифераза в Общомедия | |||||||||||
| Луцифераза от динофлагелати/N-терминален домен | |||||||||||
| Идентификатори | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Символ | Luciferase_N | ||||||||||
| Pfam | PF05295 | ||||||||||
| InterPro | IPR007959 | ||||||||||
| |||||||||||
| Луцифераза в Общомедия | |||||||||||
| Луцифераза от динофлагелати „helical bundle“ демен | |||||||||||
 Кристална структура на домен на луцифераза от динофлагелата Lingulodinium polyedrum | |||||||||||
| Идентификатори | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Символ | Luciferase_3H | ||||||||||
| Pfam | PF10284 | ||||||||||
| InterPro | IPR018475 | ||||||||||
| |||||||||||
| Луцифераза в Общомедия | |||||||||||
Механизъм на действие
редактиранеХимическата реакция, катализирана от луцифераза се провежда в два етапа:
луциферин + АТФ → луцуферил аденилат + PPi
луцуферил аденилат + O2 → оксилуциферин + АМФ + светлина
Светлина се излъчва, защото при реакцията се получва оксилуциферин в електронно възбудено състояние. Отделя се светлинен фотон връщането на оксилуциферин към основното състояние.
Луциферил аденилат може допълнително да участват в странична реакция с кислород, при което се образува водороден пероксид и дехидролуциферил-AMP. Около 20% от междинния аденилат ауциферил се окислява в този път.[2]
Реакцията се катализира от бактериална луцифераза е окислителен процес:
FMNH2 + O2 + RCHO → FMN + RCOOH + H2O + светлина
В тази реакцията, редуцираният флавин мононуклеотид (ФМН, FMN) окислява алифатен алдехид с дълга верига до алифатна карбоксилна киселина. Реакцията дава възбуден междинен хидроксифлавин, който се дехидратира до флавин мононуклеотид емититайки синьо-зелена светлина.[3]
Почти цялата енергия в реакцията се превръща в светлина. Реакцията е 80%[4] до 90%[5] ефективна. Като сравнение, електрическата крушка конвертира само около 10% от своята енергия в светлина.
Луциферазата от светулка генерира светлина от луциферин в многоетапен процес. Първо, D-луциферин се редуцира от MgATP до луциферил аденилат и пирофосфат. След активиране на АТР, луциферил аденилатът се окислява с молекулен кислород (O2), като се образува диоксетнонов пръстен. Реакция на декарбоксилиране образува възбудено състояние на оксилуциферин, които таумеризира между кето-енолна формата. Накрая се излъчва светлина като оксилуциферин се връща към основното състояние.[6]
Източници
редактиране- ↑ Gould SJ, Subramani S. Firefly luciferase as a tool in molecular and cell biology // Anal. Biochem. 175 (1). November 1988. DOI:10.1016/0003-2697(88)90353-3. с. 5 – 13.
- ↑ Fraga H, Fernandes D, Novotny J, Fontes R, Esteves da Silva JC. Firefly luciferase produces hydrogen peroxide as a coproduct in dehydroluciferyl adenylate formation // Chembiochem 7 (6). Юни 2006. DOI:10.1002/cbic.200500443. с. 929 – 35.
- ↑ Fisher AJ, Thompson TB, Thoden JB, Baldwin TO, Rayment I. The 1.5-A resolution crystal structure of bacterial luciferase in low salt conditions // J. Biol. Chem. 271 (36). Септември 1996. с. 21956 – 68.
- ↑ Elizabeth Wilson. What's That Stuff? // Chemical and Engineering News 77 (3). Jan 18, 1999. с. 65.
- ↑ Vanessa Knivett. Lighting the way // EE times. 2009.
- ↑ Baldwin TO. Firefly luciferase: the structure is known, but the mystery remains // Structure 4 (3). March 1996. DOI:10.1016/S0969-2126(96)00026-3. с. 223 – 8.